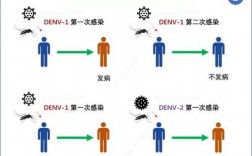
大家好!小编今天给大家解答一下有关临床医生疫苗临床试验,以及分享几个临床医生疫苗临床试验是什么对应的知识点,希望对各位有所帮助,不要忘了收藏本站喔。
临床试验的基本类型有
1、安全性试验:仅评估研究药物在试验计划的使用情况下的安全性。有效性试验:仅考量研究药物作用于疾病或健康状态的效果。安全性和有效性试验:同时考量和评价研究药物的安全性和有效性。

2、临床试验设计的五种类型包括:随机对照试验(RCT)、队列研究、病例对照研究、交叉试验和自身对照试验。随机对照试验(RCT)是临床试验设计的黄金标准。
3、个案研究——任何一种新的治疗都从个案研究开始。临床少见的疑难重症。
4、国内临床试验分为两类: 与全球同步进行的临床试验,试验药品为新药,在国内外均未上市,在全球多国同时进行临床试验研究。
5、临床研究类型包括如下:观察性研究:观察性研究是一种非干预性的研究方法,研究者通过收集和分析数据来了解疾病的发生率、流行趋势和影响因素。观察性研究又分为描述性研究和分析性研究。
首个新冠mRNA疫苗获批临床,临床试验行业有多艰辛?
月25日消息由军事医学科学院和地方企业共同研制的新型冠状病毒候选基因疫苗(ARCoV)于6月19日获得国家药品监督管理局临床试验的正式批准。这是中国第一个批准用于临床试验的新冠疫苗。
为了使得新冠疫苗用在人的身上不会有副作用,不得不进行临床试验,临床试验算是花费时间最长的,只有多次实验才能保证新冠疫苗的安全性,因为到时候会用到各国人的身上。
月19日,由军事科学院军事医学研究院与地方企业共同研发的新型冠状病毒mRNA候选疫苗(ARCoV)已正式通过国家药品监督管理局临床试验批准。这是中国国内首个获批开展临床试验的mRNA疫苗。
终于,在4月13日的时候,我国医疗团队研发的新冠灭活疫苗终于获批进入到临床试验阶段。

新款新冠病毒效果较好。根据国家最新公布的消息来看,我国最新研制的三款新冠疫苗病毒的临床实验结果还是非常完美的。毕竟能够通过临床试验批准,说明这三款疫苗的安全性非常高。
疫苗3期临床试验有多重要?
待通过III期临床试验后,疫苗即可进行批量生产。新冠疫情已经在全球范围内流行了半年多的时间,国内外多家科研机构表示我们要做好其长期存在的准备。
在此过程中对疾病的发生发展过程对药物疗效的影响进行研究;确定III期临床试验的给药剂量和方案;获得更多的药物安全性方面的资料。
也证明了疫苗的的安全有效性。三期临床试验结果的发表也证明了疫苗对人体抵抗新冠病毒感染可以提供保护。这真的是一桩值得庆祝点赞的喜事。也让我们看到了抗疫的胜利曙光。感谢那些一直默默奉献研发的人们。
临床试验阶段是疫苗研发的第二阶段,主要包括三个阶段:I期临床试验、II期临床试验和III期临床试验。这个阶段的目的是评估疫苗的安全性、免疫原性和有效性,并确定最佳的接种方案和免疫程序。
安全性好,不良反应多为注射部位疼痛,程度轻,具有一过性和自限性。从试验报告的结果中,我们能够了解到,我国三期疫苗的安全性不仅非常高,而且针对新冠病毒也有非常好的防范效果,这在全世界范围内都是非常厉害的。
疫苗临床试验需要多久,分为几个阶段?
1、通常疫苗注册上市前需经过三个阶段的临床试验,每个阶段的目标和意义不一样,根据研发的设计,方案不一样,需要的时间也不一样。
2、试验多久其实是没有定论的。正常情况下,一种新型疫苗的研发周期可能在10-15年,有时甚至更长。这样可以让研究人员充分了解这种疾病及其病原体,并确保针对这种疾病的疫苗是安全的。
3、当一种疫苗通过动物实验表现出潜在的益处后,就可以开始进行人类临床试验。临床试验通常分为三个不同的阶段(Ⅰ、Ⅱ、Ⅲ相),每个阶段都有特定的测试目标和数百名志愿者。
4、临床试验阶段是疫苗研发的第二阶段,主要包括三个阶段:I期临床试验、II期临床试验和III期临床试验。这个阶段的目的是评估疫苗的安全性、免疫原性和有效性,并确定最佳的接种方案和免疫程序。
以上内容就是解答有关临床医生疫苗临床试验的详细内容了,我相信这篇文章可以为您解决一些疑惑,有任何问题欢迎留言反馈,谢谢阅读。

 微信扫一扫打赏
微信扫一扫打赏